ค่าคงที่ของ Boltzmann เท่ากับสูตร ค่าคงที่ของ Boltzmann: ความหมายและความหมายทางกายภาพ

ตามกฎของสเตฟาน-โบลต์ซมันน์ ความหนาแน่นของรังสีในซีกโลกหนึ่ง อี 0ขึ้นอยู่กับอุณหภูมิเท่านั้นและแปรผันตามสัดส่วนกำลังสี่ของอุณหภูมิสัมบูรณ์ ต:
ค่าคงที่สเตฟาน–โบลต์ซมันน์ σ 0 เป็นค่าคงที่ทางกายภาพที่รวมอยู่ในกฎหมายที่กำหนดความหนาแน่นเชิงปริมาตรของการแผ่รังสีความร้อนที่สมดุลของวัตถุสีดำสนิท:

ในอดีต กฎสเตฟาน-โบลต์ซมันน์ถูกกำหนดขึ้นก่อนกฎรังสีของพลังค์ ซึ่งตามมาด้วยผลที่ตามมา กฎของพลังค์กำหนดความขึ้นอยู่กับความหนาแน่นของฟลักซ์สเปกตรัมของรังสี อี 0 เกี่ยวกับความยาวคลื่น แลมบ์ และอุณหภูมิ ต:

โดยที่ λ – ความยาวคลื่น, m; กับ=2.998 10 8 m/s – ความเร็วแสงในสุญญากาศ; ต– อุณหภูมิร่างกาย K;
ชม.= 6.625 ×10 -34 J×s – ค่าคงที่ของพลังค์
ค่าคงที่ทางกายภาพ เคเท่ากับอัตราส่วนของค่าคงที่ก๊าซสากล ร=8314J/(kg×K) เท่ากับเลขอาโวกาโดร เอ็น.เอ.=6.022× 10 26 1/(กก.×โมล):
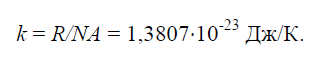
จำนวนการกำหนดค่าระบบที่แตกต่างกัน เอ็นอนุภาคสำหรับชุดตัวเลขที่กำหนด ฉัน(จำนวนอนุภาคใน ฉัน- สถานะที่พลังงาน e i สอดคล้องกัน) เป็นสัดส่วนกับค่า:

ขนาด วมีหลายวิธีในการกระจาย เอ็นอนุภาคตามระดับพลังงาน หากความสัมพันธ์ (6) เป็นจริง จะถือว่าระบบเดิมเป็นไปตามสถิติของ Boltzmann ชุดตัวเลข ฉันซึ่งจำนวนนั้น วสูงสุด เกิดขึ้นบ่อยที่สุดและสอดคล้องกับการแจกแจงที่เป็นไปได้มากที่สุด
จลนศาสตร์ทางกายภาพ– ทฤษฎีจุลทรรศน์ของกระบวนการในระบบที่ไม่มีความสมดุลทางสถิติ
การอธิบายอนุภาคจำนวนมากสามารถทำได้สำเร็จโดยใช้วิธีความน่าจะเป็น สำหรับก๊าซ monatomic สถานะของชุดโมเลกุลจะถูกกำหนดโดยพิกัดและค่าของการประมาณการความเร็วบนแกนพิกัดที่สอดคล้องกัน ในทางคณิตศาสตร์ สิ่งนี้อธิบายได้ด้วยฟังก์ชันการแจกแจง ซึ่งระบุลักษณะความน่าจะเป็นที่อนุภาคจะเข้าไป รัฐนี้:

คือจำนวนโมเลกุลที่คาดหวังในปริมาตร d d ซึ่งมีพิกัดอยู่ในช่วงตั้งแต่ถึง +d และมีความเร็วอยู่ในช่วงตั้งแต่ถึง +d
หากสามารถละเลยพลังงานศักย์เฉลี่ยตามเวลาของปฏิกิริยาของโมเลกุลเมื่อเปรียบเทียบกับพลังงานจลน์ของพวกมัน ก๊าซนั้นจะถูกเรียกว่าอุดมคติ ก๊าซในอุดมคติเรียกว่าก๊าซโบลต์ซมันน์ หากอัตราส่วนของความยาวเส้นทางของโมเลกุลในก๊าซนี้ต่อขนาดลักษณะเฉพาะของการไหล ลแน่นอน กล่าวคือ

เพราะ ความยาวเส้นทางเป็นสัดส่วนผกผัน อันดับ 2(n คือความหนาแน่นเชิงตัวเลข 1/m 3, d คือเส้นผ่านศูนย์กลางของโมเลกุล, m)
ขนาด
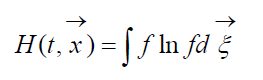
เรียกว่า ชม-ฟังก์ชัน Boltzmann สำหรับหน่วยปริมาตร ซึ่งสัมพันธ์กับความน่าจะเป็นในการตรวจจับระบบโมเลกุลของก๊าซในสถานะที่กำหนด แต่ละสถานะสอดคล้องกับจำนวนเซลล์ความเร็วอวกาศหกมิติที่เติมเข้าไป ซึ่งสามารถแบ่งช่องว่างเฟสของโมเลกุลที่กำลังพิจารณาได้ มาแสดงกันเถอะ วความน่าจะเป็นที่จะมีโมเลกุล N 1 ในเซลล์แรกของช่องว่างที่พิจารณา, N 2 ในเซลล์ที่สอง เป็นต้น
จนถึงค่าคงที่ที่กำหนดที่มาของความน่าจะเป็น ความสัมพันธ์ต่อไปนี้ใช้ได้:
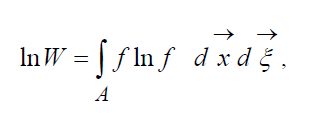 ,
,
ที่ไหน  – ฟังก์ชัน H ของขอบเขตพื้นที่ กครอบครองโดยก๊าซ จาก (9) ชัดเจนว่า วและ ชมเชื่อมต่อกันเช่น การเปลี่ยนแปลงความน่าจะเป็นของสถานะจะนำไปสู่การวิวัฒนาการที่สอดคล้องกันของฟังก์ชัน H
– ฟังก์ชัน H ของขอบเขตพื้นที่ กครอบครองโดยก๊าซ จาก (9) ชัดเจนว่า วและ ชมเชื่อมต่อกันเช่น การเปลี่ยนแปลงความน่าจะเป็นของสถานะจะนำไปสู่การวิวัฒนาการที่สอดคล้องกันของฟังก์ชัน H
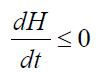
หลักการของ Boltzmann สร้างความเชื่อมโยงระหว่างเอนโทรปี สระบบทางกายภาพและความน่าจะเป็นทางอุณหพลศาสตร์ วรัฐของเธอ:

(เผยแพร่ตามสิ่งพิมพ์: Kogan M.N. พลศาสตร์ของก๊าซทำให้บริสุทธิ์ - M.: Nauka, 1967.)
มุมมองทั่วไปของ CUBE:

แรงมวลอยู่ที่ไหนเนื่องจากการมีอยู่ของสนามต่าง ๆ (แรงโน้มถ่วง, ไฟฟ้า, แม่เหล็ก) ที่กระทำต่อโมเลกุล เจ– อินทิกรัลการชนกัน มันเป็นเทอมของสมการ Boltzmann นี้ที่คำนึงถึงการชนกันของโมเลกุลซึ่งกันและกันและการเปลี่ยนแปลงความเร็วของอนุภาคที่มีปฏิสัมพันธ์กัน อินทิกรัลการชนกันเป็นอินทิกรัลห้ามิติและมีโครงสร้างดังนี้

ได้รับสมการ (12) กับอินทิกรัล (13) สำหรับการชนของโมเลกุลที่ไม่มีแรงสัมผัสเกิดขึ้นเช่น อนุภาคที่ชนกันถือว่ามีความเรียบอย่างสมบูรณ์แบบ
ในระหว่างการโต้ตอบพลังงานภายในของโมเลกุลจะไม่เปลี่ยนแปลงเช่น โมเลกุลเหล่านี้ถือว่ายืดหยุ่นได้อย่างสมบูรณ์แบบ พิจารณาโมเลกุลสองกลุ่มโดยมีความเร็วและก่อนชนกัน (การชนกัน) และหลังจากการชนตามลำดับความเร็วและ ความแตกต่างของความเร็วเรียกว่าความเร็วสัมพัทธ์เช่น . เห็นได้ชัดว่าเพื่อการชนแบบยืดหยุ่นที่ราบรื่น ฟังก์ชันการกระจาย ฉ 1 ", ฉ", ฉ 1 , ฉอธิบายโมเลกุลของกลุ่มที่เกี่ยวข้องหลังและก่อนการชนเช่น ![]() ;
; ![]() ;
; ![]() ;
; ![]() .
.

ข้าว. 1. การชนกันของโมเลกุลทั้งสอง
(13) รวมถึงพารามิเตอร์สองตัวที่แสดงคุณลักษณะตำแหน่งของโมเลกุลที่ชนกันซึ่งสัมพันธ์กัน: ขและ ε; ข– ระยะการเล็ง เช่น ระยะทางที่เล็กที่สุดที่โมเลกุลจะเข้าใกล้ในกรณีที่ไม่มีปฏิสัมพันธ์ (รูปที่ 2) ε เรียกว่าพารามิเตอร์เชิงมุมของการชนกัน (รูปที่ 3) บูรณาการมากกว่า ขจาก 0 ถึง ¥ และจาก 0 ถึง 2p (อินทิกรัลภายนอกสองตัวใน (12)) ครอบคลุมระนาบปฏิสัมพันธ์ของแรงทั้งหมดที่ตั้งฉากกับเวกเตอร์

ข้าว. 2. วิถีโคจรของโมเลกุล

ข้าว. 3. การพิจารณาปฏิสัมพันธ์ของโมเลกุลในระบบพิกัดทรงกระบอก: z, ข, ε
สมการจลนศาสตร์ของ Boltzmann ได้มาจากสมมติฐานและสมมติฐานต่อไปนี้
1. เชื่อกันว่าการชนกันของโมเลกุลทั้งสองส่วนใหญ่เกิดขึ้น กล่าวคือ บทบาทของการชนกันของทั้งสามและพร้อมกัน มากกว่าโมเลกุลไม่มีนัยสำคัญ สมมติฐานนี้ช่วยให้เราสามารถใช้ฟังก์ชันการกระจายอนุภาคเดี่ยวสำหรับการวิเคราะห์ ซึ่งข้างต้นเรียกง่ายๆ ว่าฟังก์ชันการกระจาย เมื่อคำนึงถึงการชนกันของโมเลกุลทั้งสามทำให้จำเป็นต้องใช้ฟังก์ชันการกระจายอนุภาคแบบสองอนุภาคในการศึกษานี้ ดังนั้นการวิเคราะห์จึงมีความซับซ้อนมากขึ้นอย่างมาก
2. การสันนิษฐานของความสับสนวุ่นวายระดับโมเลกุล แสดงให้เห็นข้อเท็จจริงที่ว่าความน่าจะเป็นในการตรวจจับอนุภาค 1 ที่จุดเฟสและอนุภาค 2 ที่จุดเฟสนั้นเป็นอิสระจากกัน
3. การชนกันของโมเลกุลที่มีระยะการกระแทกมีความเป็นไปได้เท่ากัน กล่าวคือ ฟังก์ชันการกระจายไม่เปลี่ยนแปลงที่เส้นผ่านศูนย์กลางปฏิสัมพันธ์ ควรสังเกตว่าองค์ประกอบที่วิเคราะห์จะต้องมีขนาดเล็กเช่นนั้น ฉภายในองค์ประกอบนี้ไม่เปลี่ยนแปลง แต่ในขณะเดียวกันเพื่อให้ความผันผวนของสัมพัทธ์ ~ ไม่มาก ศักยภาพในการโต้ตอบที่ใช้ในการคำนวณอินทิกรัลการชนนั้นมีความสมมาตรแบบทรงกลม เช่น ![]() .
.
การกระจายของแม็กซ์เวลล์-โบลต์ซมันน์
สถานะสมดุลของก๊าซอธิบายได้ด้วยการกระจายตัวของแมกซ์เวลเลียนสัมบูรณ์ ซึ่งเป็นวิธีแก้ปัญหาที่แน่นอน สมการจลนศาสตร์โบลต์ซมันน์:

โดยที่ m คือมวลของโมเลกุล กิโลกรัม
การแจกแจงแบบแมกซ์เวลเลียนในท้องถิ่นทั่วไป หรือเรียกอีกอย่างว่าการแจกแจงแบบแมกซ์เวลล์-โบลต์ซมันน์:

ในกรณีที่ก๊าซเคลื่อนที่โดยรวมด้วยความเร็วและตัวแปร n, T ขึ้นอยู่กับพิกัด
และเวลา t
ในสนามโน้มถ่วงของโลก ผลเฉลยที่แน่นอนของสมการโบลต์ซมันน์แสดงให้เห็นว่า:

ที่ไหน n 0 = ความหนาแน่นที่พื้นผิวโลก 1/ลบ.ม. ก– ความเร่งด้วยแรงโน้มถ่วง, m/s 2 ; ชม.– ความสูง, m สูตร (16) เป็นคำตอบที่แน่นอนของสมการจลน์ศาสตร์ของ Boltzmann ในพื้นที่ไม่จำกัดหรือในขอบเขตที่ไม่ละเมิดการกระจายนี้ ในขณะที่อุณหภูมิก็ต้องคงที่เช่นกัน
หน้านี้ออกแบบโดย Puzina Yu.Yu สนับสนุนโดย มูลนิธิรัสเซียการวิจัยขั้นพื้นฐาน – โครงการที่ 08-08-00638.
ตั้งชื่อตามนักฟิสิกส์ชาวออสเตรีย ลุดวิก โบลต์ซมันน์ ซึ่งมีส่วนสำคัญในวิชาฟิสิกส์เชิงสถิติ โดยค่าคงที่นี้มีบทบาทสำคัญ ค่าทดลองในระบบ SI คือ
เจ/.ตัวเลขในวงเล็บแสดงถึงข้อผิดพลาดมาตรฐานในหลักสุดท้ายของค่าปริมาณ โดยหลักการแล้ว ค่าคงที่ของโบลต์ซมันน์สามารถหาได้จากคำนิยามของอุณหภูมิสัมบูรณ์และค่าคงที่ทางกายภาพอื่นๆ อย่างไรก็ตาม การคำนวณค่าคงที่ของ Boltzmann โดยใช้หลักการแรกนั้นซับซ้อนเกินไปและเป็นไปไม่ได้กับสถานะความรู้ในปัจจุบัน ในระบบธรรมชาติของหน่วยพลังค์ จะมีการกำหนดหน่วยอุณหภูมิตามธรรมชาติเพื่อให้ค่าคงที่ของโบลต์ซมันน์เท่ากับความสามัคคี
ความสัมพันธ์ระหว่างอุณหภูมิและพลังงาน
ในก๊าซอุดมคติที่เป็นเนื้อเดียวกันที่อุณหภูมิสัมบูรณ์ ตพลังงานต่อระดับความเป็นอิสระในการแปลแต่ละระดับจะเท่ากัน ดังนี้ จากการกระจายตัวของแมกซ์เวลล์ เคต/ 2 . ที่อุณหภูมิห้อง (300 ) พลังงานนี้คือ ![]() เจ หรือ 0.013 eV ในก๊าซอุดมคติแบบอะตอมเดี่ยว แต่ละอะตอมมีระดับความเป็นอิสระสามระดับซึ่งสอดคล้องกับแกนเชิงพื้นที่สามแกน ซึ่งหมายความว่าแต่ละอะตอมมีพลังงาน 3/2( เคต)
.
เจ หรือ 0.013 eV ในก๊าซอุดมคติแบบอะตอมเดี่ยว แต่ละอะตอมมีระดับความเป็นอิสระสามระดับซึ่งสอดคล้องกับแกนเชิงพื้นที่สามแกน ซึ่งหมายความว่าแต่ละอะตอมมีพลังงาน 3/2( เคต)
.
รู้ พลังงานความร้อนเราสามารถคำนวณความเร็วเฉลี่ยรากของอะตอมซึ่งเป็นสัดส่วนผกผันได้ รากที่สอง มวลอะตอม. ความเร็วกำลังสองเฉลี่ยรากที่อุณหภูมิห้องแปรผันจาก 1370 m/s สำหรับฮีเลียม ถึง 240 m/s สำหรับซีนอน ในกรณีของก๊าซโมเลกุล สถานการณ์จะซับซ้อนมากขึ้น เช่น ก๊าซไดอะตอมมิกมีระดับความอิสระประมาณห้าระดับอยู่แล้ว
ความหมายของเอนโทรปี
เอนโทรปี ระบบอุณหพลศาสตร์กำหนดให้เป็นลอการิทึมธรรมชาติของจำนวนไมโครสเตตต่างๆ ซีซึ่งสอดคล้องกับสถานะมหภาคที่กำหนด (เช่น สถานะที่มีพลังงานทั้งหมดที่กำหนด)
ส = เค ln ซี.ปัจจัยสัดส่วน เคและเป็นค่าคงที่ของ Boltzmann นี่คือการแสดงออกที่กำหนดความสัมพันธ์ระหว่างกล้องจุลทรรศน์ ( ซี) และสถานะมหภาค ( ส) เป็นการแสดงออกถึงแนวคิดหลักของกลศาสตร์ทางสถิติ
ดูสิ่งนี้ด้วย
มูลนิธิวิกิมีเดีย 2010.
ดูว่า "ค่าคงที่ของ Boltzmann" ในพจนานุกรมอื่น ๆ คืออะไร:
- จักรวาลและฟิสิกส์ที่ไม่มี “พลังงานมืด” (การค้นพบ ความคิด สมมติฐาน) ใน 2 เล่ม เล่มที่ 1 O. G. Smirnov หนังสือเล่มนี้อุทิศให้กับปัญหาฟิสิกส์และดาราศาสตร์ที่มีอยู่ในวิทยาศาสตร์มาเป็นเวลาหลายสิบปีตั้งแต่ G. Galileo, I. Newton, A. Einstein จนถึงปัจจุบัน อนุภาคที่เล็กที่สุดของสสารและดาวเคราะห์ ดวงดาว และ...
ค่าคงที่ทางกายภาพ k เท่ากับอัตราส่วนของค่าคงที่ก๊าซสากล R ต่อเลขอาโวกาโดร NA: k = R/NA = 1.3807.10 23 J/K ตั้งชื่อตาม L. Boltzmann... ใหญ่ พจนานุกรมสารานุกรม
ค่าคงที่ทางกายภาพพื้นฐานอย่างหนึ่ง เท่ากับอัตราส่วนของค่าคงที่ของก๊าซ R ต่อค่าคงที่ Avogadro NA ซึ่งเขียนแทนด้วย k; ตั้งชื่อตามชาวออสเตรีย นักฟิสิกส์ แอล. โบลต์ซมันน์ bp รวมอยู่ในความสัมพันธ์ที่สำคัญที่สุดของฟิสิกส์จำนวนหนึ่ง: ในสมการ... ... สารานุกรมทางกายภาพ
โบลซ์มันน์ คอนสแตนต์- (k) กายภาพสากล ค่าคงที่เท่ากับอัตราส่วนของก๊าซสากล (ดู) ต่อค่าคงที่ Avogadro NA: k = R/Na = (1.380658 ± 000012)∙10 23 J/K ... สารานุกรมโพลีเทคนิคขนาดใหญ่
ค่าคงที่ทางกายภาพ k เท่ากับอัตราส่วนของค่าคงที่ก๊าซสากล R ต่อเลขอาโวกาโดร NA: k = R/NA = 1.3807·10 23 J/K ตั้งชื่อตามแอล. โบลทซ์มันน์ * * * ค่าคงที่ของ BOLTZMANN ค่าคงที่ของ BOLTZMANN ค่าคงที่ทางกายภาพ k เท่ากับ... ... พจนานุกรมสารานุกรม
ฟิสิกส์ ค่าคงที่ k เท่ากับอัตราส่วนของสากล ค่าคงที่ของก๊าซ R เท่ากับเลขอาโวกาโดร NA: k = R/NA = 1.3807 x 10 23 J/K ตั้งชื่อตาม L. Boltzmann... วิทยาศาสตร์ธรรมชาติ. พจนานุกรมสารานุกรม
ค่าคงที่ทางกายภาพพื้นฐานค่าหนึ่ง (ดูค่าคงที่ทางกายภาพ) เท่ากับอัตราส่วนของค่าคงที่ก๊าซสากล R ต่อเลข Avogadro NA (จำนวนโมเลกุลใน 1 โมลหรือ 1 กิโลเมตรโมลของสาร): k = R/NA ตั้งชื่อตามแอล. โบลทซ์มันน์ บีพี.... ... สารานุกรมผู้ยิ่งใหญ่แห่งสหภาพโซเวียต
(เคหรือ เคข)เป็นค่าคงที่ทางกายภาพที่กำหนดความสัมพันธ์ระหว่างอุณหภูมิและพลังงาน ตั้งชื่อตามนักฟิสิกส์ชาวออสเตรีย ลุดวิก โบลต์ซมันน์ ผู้มีส่วนสำคัญในวิชาฟิสิกส์เชิงสถิติ ซึ่งสิ่งนี้กลายเป็นตำแหน่งสำคัญ ค่าทดลองในระบบ SI คือตัวเลขในวงเล็บแสดงถึงข้อผิดพลาดมาตรฐานในหลักสุดท้ายของค่าปริมาณ โดยหลักการแล้ว ค่าคงที่ของ Boltzmann สามารถหาได้จากคำจำกัดความของอุณหภูมิสัมบูรณ์และค่าคงที่ทางกายภาพอื่นๆ (ในการทำเช่นนี้ คุณจะต้องสามารถคำนวณอุณหภูมิของจุดสามจุดของน้ำได้จากหลักการแรก) แต่การกำหนดค่าคงที่ของ Boltzmann โดยใช้หลักการแรกนั้นซับซ้อนเกินไปและไม่สมจริงเมื่อใด การพัฒนาที่ทันสมัยความรู้ในด้านนี้
ค่าคงที่ของ Boltzmann– ค่าคงที่ทางกายภาพที่มากเกินไปหากคุณวัดอุณหภูมิในหน่วยพลังงาน ซึ่งมักทำในวิชาฟิสิกส์ อันที่จริงมันคือความเชื่อมโยงระหว่างปริมาณที่กำหนดไว้อย่างชัดเจน - พลังงานและระดับ ซึ่งเป็นความหมายที่พัฒนาขึ้นในอดีต
ความหมายของเอนโทรปี
เอนโทรปีของระบบอุณหพลศาสตร์ถูกกำหนดให้เป็นลอการิทึมธรรมชาติของจำนวนไมโครสเตต Z ที่แตกต่างกันซึ่งสอดคล้องกับสถานะมหภาคที่กำหนด (ตัวอย่างเช่น สถานะที่มีพลังงานทั้งหมดที่กำหนด)
ปัจจัยสัดส่วน เคและเป็นค่าคงที่ของ Boltzmann การแสดงออกนี้ซึ่งกำหนดความสัมพันธ์ระหว่างลักษณะกล้องจุลทรรศน์ (Z) และลักษณะมหภาค (S) เป็นการแสดงออกถึงแนวคิดหลัก (ส่วนกลาง) ของกลศาสตร์ทางสถิติ
ความสัมพันธ์ที่กำหนดระหว่างอุณหภูมิและพลังงาน ตั้งชื่อตามนักฟิสิกส์ชาวออสเตรีย ลุดวิก โบลต์ซมันน์ ซึ่งมีส่วนสำคัญในวิชาฟิสิกส์เชิงสถิติ โดยค่าคงที่นี้มีบทบาทสำคัญ ค่าทดลองในระบบหน่วยสากล (SI) คือ:
เจ/.ตัวเลขในวงเล็บแสดงถึงข้อผิดพลาดมาตรฐานในหลักสุดท้ายของค่าปริมาณ ค่าคงที่ของโบลต์ซมันน์สามารถหาได้จากคำจำกัดความของอุณหภูมิสัมบูรณ์และค่าคงที่ทางกายภาพอื่นๆ อย่างไรก็ตาม การคำนวณค่าคงที่ของ Boltzmann โดยใช้หลักการแรกนั้นซับซ้อนเกินไปและเป็นไปไม่ได้กับสถานะความรู้ในปัจจุบัน ในระบบธรรมชาติของหน่วยพลังค์ จะมีการกำหนดหน่วยอุณหภูมิตามธรรมชาติเพื่อให้ค่าคงที่ของโบลต์ซมันน์เท่ากับความสามัคคี
ความสัมพันธ์ระหว่างอุณหภูมิและพลังงาน
ในก๊าซอุดมคติที่เป็นเนื้อเดียวกันที่อุณหภูมิสัมบูรณ์ พลังงานต่อระดับความอิสระในการแปลแต่ละระดับจะเป็นดังนี้จากการกระจายตัวของแมกซ์เวลล์ ที่อุณหภูมิห้อง (300°C) พลังงานนี้คือ J หรือ 0.013 eV ในก๊าซอุดมคติเชิงเดี่ยว แต่ละอะตอมมีระดับความอิสระสามระดับซึ่งสอดคล้องกับแกนเชิงพื้นที่สามแกน ซึ่งหมายความว่าแต่ละอะตอมมีพลังงานเท่ากับ
เมื่อทราบพลังงานความร้อนแล้ว เราสามารถคำนวณความเร็วเฉลี่ยกำลังสองของรากของอะตอมได้ ซึ่งเป็นสัดส่วนผกผันกับรากที่สองของมวลอะตอม ความเร็วกำลังสองเฉลี่ยรากที่อุณหภูมิห้องแปรผันจาก 1370 m/s สำหรับฮีเลียม ถึง 240 m/s สำหรับซีนอน ในกรณีของก๊าซโมเลกุล สถานการณ์จะซับซ้อนมากขึ้น เช่น ก๊าซไดอะตอมมิกมีระดับความอิสระประมาณห้าระดับ
ความหมายของเอนโทรปี
เอนโทรปีของระบบอุณหพลศาสตร์ถูกกำหนดให้เป็นลอการิทึมธรรมชาติของจำนวนไมโครสเตตที่แตกต่างกันซึ่งสอดคล้องกับสถานะมหภาคที่กำหนด (ตัวอย่างเช่น สถานะที่มีพลังงานทั้งหมดที่กำหนด)
ค่าสัมประสิทธิ์สัดส่วนคือค่าคงที่ของ Boltzmann การแสดงออกนี้ซึ่งกำหนดความสัมพันธ์ระหว่างกล้องจุลทรรศน์ () และสถานะมหภาค () เป็นการแสดงออกถึงแนวคิดหลักของกลศาสตร์ทางสถิติ
ดูสิ่งนี้ด้วย
หมายเหตุ
มูลนิธิวิกิมีเดีย 2010.
ดูว่า "ค่าคงที่ของ Boltzmann" ในพจนานุกรมอื่น ๆ คืออะไร:
- (สัญลักษณ์ k) อัตราส่วนของค่าคงที่ GAS สากลต่อ AVOGADRO NUMBER เท่ากับ 1.381.10 23 จูลต่อองศาเคลวิน มันบ่งบอกถึงความสัมพันธ์ระหว่างพลังงานจลน์ของอนุภาคก๊าซ (อะตอมหรือโมเลกุล) กับอุณหภูมิสัมบูรณ์.... ... พจนานุกรมสารานุกรมวิทยาศาสตร์และเทคนิค
ค่าคงที่ของโบลทซ์มันน์- - [เอเอส โกลด์เบิร์ก พจนานุกรมพลังงานภาษาอังกฤษเป็นภาษารัสเซีย 2549] หัวข้อพลังงานโดยทั่วไปค่าคงที่ของ EN Boltzmann ... คู่มือนักแปลด้านเทคนิค
ค่าคงที่ของ Boltzmann- ค่าคงที่ของ Boltzmann ค่าคงที่ของ Boltzmann ค่าคงที่ทางกายภาพที่กำหนดความสัมพันธ์ระหว่างอุณหภูมิและพลังงาน ตั้งชื่อตามนักฟิสิกส์ชาวออสเตรีย ลุดวิก โบลต์ซมันน์ ผู้สร้างคุณูปการสำคัญให้กับฟิสิกส์เชิงสถิติ ซึ่งค่าคงที่นี้ ... อธิบาย พจนานุกรมภาษาอังกฤษเป็นภาษารัสเซียเกี่ยวกับนาโนเทคโนโลยี - ม.
ค่าคงที่ของโบลทซ์มันน์- Bolcmano konstanta statusas T sritis fizika atitikmenys: อังกฤษ vok คงที่ของ Boltzmann โบลต์ซมันน์ คอนสแตนเต้, f; โบลต์ซมันน์เชอ คอนสแตนเต, รัสเซี่ยน. ค่าคงที่ Boltzmann, f pran Constante de Boltzmann, f … Fizikos สิ้นสุด žodynas
ความสัมพันธ์ S k lnW ระหว่างเอนโทรปี S และความน่าจะเป็นทางอุณหพลศาสตร์ W (ค่าคงที่ k Boltzmann) การตีความทางสถิติของกฎข้อที่สองของอุณหพลศาสตร์เป็นไปตามหลักการของ Boltzmann: กระบวนการทางธรรมชาติพยายามแปลอุณหพลศาสตร์......
- (การกระจายของ Maxwell Boltzmann) การกระจายสมดุลของอนุภาคก๊าซในอุดมคติด้วยพลังงาน (E) ในสนามแรงภายนอก (เช่น ในสนามโน้มถ่วง) ถูกกำหนดโดยฟังก์ชันการกระจาย f e E/kT โดยที่ E คือผลรวมของพลังงานจลน์และพลังงานศักย์... พจนานุกรมสารานุกรมขนาดใหญ่
อย่าสับสนกับค่าคงที่ของ Boltzmann ค่าคงที่ของสเตฟาน โบลต์ซมันน์ (รวมถึงค่าคงที่ของสเตฟานด้วย) ค่าคงที่ทางกายภาพที่เป็นค่าคงที่ของสัดส่วนในกฎของสเตฟาน โบลต์ซมันน์: พลังงานทั้งหมดที่ปล่อยออกมาต่อหน่วยพื้นที่... Wikipedia
ค่าคงที่ มิติ 1.380 6504(24)×10−23 J K−1 8.617 343(15)×10−5 eV K−1 1.3807×10−16 erg K−1 ค่าคงที่ Boltzmann (k หรือ kb) ค่าคงที่ทางกายภาพที่ กำหนดความสัมพันธ์ระหว่างอุณหภูมิและพลังงาน ตั้งชื่อตามชาวออสเตรีย... ... Wikipedia
การกระจายสมดุลทางสถิติทำหน้าที่เหนือโมเมนต้าและพิกัดของอนุภาคของก๊าซในอุดมคติ ซึ่งโมเลกุลเป็นไปตามรูปแบบคลาสสิก กลศาสตร์ในสนามศักย์ภายนอก: นี่คือค่าคงที่ของโบลต์ซมันน์ (ค่าคงที่สากล) สัมบูรณ์... ... สารานุกรมคณิตศาสตร์
