ความร้อนจำเพาะของการระเหยของการกลายเป็นไอ ความร้อนแฝงของการกลายเป็นไอ
เรียกว่าปรากฏการณ์ของสารที่เปลี่ยนจากของเหลวเป็นสถานะก๊าซ การกลายเป็นไอ- การกลายเป็นไอสามารถดำเนินการได้ในรูปแบบของสองกระบวนการ:
เดือด
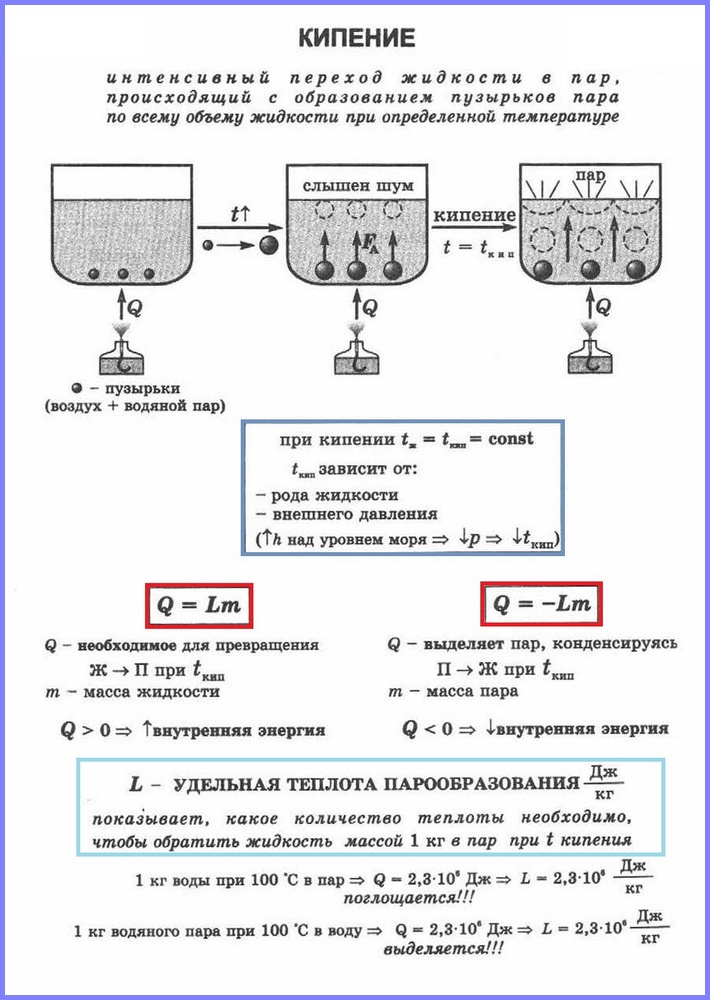
กระบวนการที่สองของการกลายเป็นไอคือการเดือด กระบวนการนี้สามารถสังเกตได้โดยใช้การทดลองง่ายๆ โดยให้ความร้อนน้ำในขวดแก้ว เมื่อน้ำร้อนฟองอากาศจะปรากฏขึ้นหลังจากนั้นไม่นานซึ่งมีอากาศและไอน้ำอิ่มตัวซึ่งเกิดขึ้นเมื่อน้ำระเหยภายในฟองอากาศ เมื่ออุณหภูมิสูงขึ้น ความดันภายในฟองอากาศจะเพิ่มขึ้น และภายใต้อิทธิพลของแรงลอยตัว ฟองอากาศก็จะลอยขึ้นด้านบน อย่างไรก็ตาม เนื่องจากอุณหภูมิของน้ำชั้นบนต่ำกว่าอุณหภูมิด้านล่าง ไอในฟองอากาศจึงเริ่มควบแน่นและหดตัว เมื่อน้ำอุ่นขึ้นตลอดปริมาตร ฟองที่มีไอน้ำจะลอยขึ้นสู่ผิวน้ำ ระเบิด และไอน้ำจะออกมา น้ำกำลังเดือด สิ่งนี้เกิดขึ้นที่อุณหภูมิซึ่งความดันไออิ่มตัวในฟองอากาศเท่ากับความดันบรรยากาศ
กระบวนการกลายเป็นไอที่เกิดขึ้นในปริมาตรของเหลวทั้งหมดที่อุณหภูมิหนึ่งเรียกว่า อุณหภูมิที่ของเหลวเดือดเรียกว่า จุดเดือด.
อุณหภูมินี้ขึ้นอยู่กับความดันบรรยากาศ เมื่อความดันบรรยากาศเพิ่มขึ้น จุดเดือดจะเพิ่มขึ้น
ประสบการณ์แสดงให้เห็นว่าในระหว่างกระบวนการเดือด อุณหภูมิของของเหลวจะไม่เปลี่ยนแปลง แม้ว่าพลังงานจะมาจากภายนอกก็ตาม การเปลี่ยนของเหลวเป็นสถานะก๊าซที่จุดเดือดนั้นสัมพันธ์กับการเพิ่มระยะห่างระหว่างโมเลกุลและตามด้วยการเอาชนะแรงดึงดูดระหว่างพวกมัน พลังงานที่จ่ายให้กับของเหลวนั้นถูกใช้ไปเพื่อทำงานเพื่อเอาชนะแรงดึงดูด สิ่งนี้เกิดขึ้นจนกระทั่งของเหลวทั้งหมดกลายเป็นไอน้ำ เนื่องจากของเหลวและไอมีอุณหภูมิเท่ากันในระหว่างการเดือด พลังงานจลน์เฉลี่ยของโมเลกุลจึงไม่เปลี่ยนแปลง มีเพียงพลังงานศักย์เท่านั้นที่เพิ่มขึ้น
รูปนี้แสดงกราฟของอุณหภูมิของน้ำเทียบกับเวลาระหว่างการให้ความร้อนจากอุณหภูมิห้องถึงจุดเดือด (AB) จุดเดือด (BC) การให้ความร้อนด้วยไอน้ำ (CD) การทำความเย็นด้วยไอน้ำ (DE) การควบแน่น (EF) และการทำความเย็นที่ตามมา (เอฟจี).
ความร้อนจำเพาะของการกลายเป็นไอ
ในการเปลี่ยนสารต่างๆ จากของเหลวเป็นสถานะก๊าซ จำเป็นต้องใช้พลังงานที่แตกต่างกัน พลังงานนี้มีลักษณะเป็นค่าที่เรียกว่าความร้อนจำเพาะของการกลายเป็นไอ
ความร้อนจำเพาะการกลายเป็นไอ (ล) คือค่าเท่ากับอัตราส่วนของปริมาณความร้อนที่ต้องให้กับสารที่มีน้ำหนัก 1 กิโลกรัม เพื่อเปลี่ยนจากสถานะของเหลวเป็นสถานะก๊าซที่จุดเดือด
หน่วยความร้อนจำเพาะของการกลายเป็นไอ - [ ล] = เจ/กก.
ในการคำนวณปริมาณความร้อน Q ที่ต้องให้กับสารที่มีมวล mn สำหรับการเปลี่ยนจากของเหลวเป็นสถานะก๊าซ ความร้อนจำเพาะของการกลายเป็นไอ ( ล) คูณด้วยมวลของสาร: ถาม = ลม.
เมื่อไอน้ำควบแน่น ความร้อนจำนวนหนึ่งจะถูกปล่อยออกมา และค่าของมันจะเท่ากับปริมาณความร้อนที่ต้องใช้เพื่อแปลงของเหลวให้เป็นไอน้ำที่อุณหภูมิเดียวกัน

กลับไปข้างหน้า
ความสนใจ! การแสดงตัวอย่างสไลด์มีวัตถุประสงค์เพื่อให้ข้อมูลเท่านั้น และอาจไม่ได้แสดงถึงคุณลักษณะทั้งหมดของการนำเสนอ หากคุณสนใจ งานนี้โปรดดาวน์โหลดเวอร์ชันเต็ม
ประเภทของบทเรียน: รวม
ประเภทบทเรียน:การเรียนรู้เนื้อหาใหม่
เป้า:สร้างแนวคิดของการต้มเป็นการระเหย ระบุและอธิบายลักษณะการต้ม
งาน:
ทางการศึกษา:
- การก่อตัวของแนวคิดเรื่อง "การเดือด" และ "ความร้อนจำเพาะของการกลายเป็นไอและการควบแน่น"
- การระบุคุณสมบัติหลักของการเดือด: การก่อตัวของฟองอากาศ, เสียงก่อนจุดเดือด, ความคงตัวของจุดเดือดและการพึ่งพาอุณหภูมิเดือดกับความดันภายนอก
- พัฒนาความสามารถในการประยุกต์ความรู้ที่มีอยู่มาอธิบายปรากฏการณ์การระเหยและการเดือด
ทางการศึกษา:
- การพัฒนาทักษะทางปัญญา: วิเคราะห์ เปรียบเทียบ เน้นสิ่งสำคัญ และสรุปผล
- การพัฒนา การคิดเชิงตรรกะและความสนใจทางการศึกษา
ทางการศึกษา:
- การพัฒนาความสนใจในวิชาและทัศนคติเชิงบวกต่อการเรียนรู้
- การก่อตัวของโลกทัศน์ทางวิทยาศาสตร์
- ส่งเสริมความสนิทสนมกันและการช่วยเหลือซึ่งกันและกัน
การสาธิต:
- การสังเกตขั้นตอนการเดือด
- การสังเกตการพึ่งพาอุณหภูมิเดือดกับความดันภายนอก
- การสังเกตการเดือดที่ความดันลดลง
- วีดีโอ “การต้มไนโตรเจน”
อุปกรณ์: ตะเกียงแอลกอฮอล์, ขวดพร้อมน้ำ, เทอร์โมมิเตอร์สำหรับวัดอุณหภูมิของเหลว, ขาตั้ง, จุกสำหรับขวดที่มีหลอดแก้วเสียบอยู่, ท่อยาง, เข็มฉีดยา, ปั๊ม Komovsky, คอมพิวเตอร์และเครื่องฉายมัลติมีเดีย, การนำเสนอ
ความคืบหน้าของบทเรียน
1. ช่วงเวลาขององค์กร
2. แรงจูงใจ
ครู:ฉันไม่สงสัยเลยว่าทุกเช้าจะเริ่มต้นด้วยชาร้อนที่ชงมาอย่างดี ชาเป็นเครื่องดื่มเพื่อสุขภาพ - ภูมิปัญญาโบราณกล่าวเช่นนั้น และแน่นอนว่าคุณรู้ว่าก่อนที่คุณจะชงชาคุณต้องต้มน้ำก่อน โปรดใส่ใจกับ epigraph (สไลด์ 2):
“มีปรากฏการณ์ต่างๆ มากมายที่คุณไม่เคยเบื่อที่จะมองดู น้ำเดือด - เพลิดเพลินกับปรากฏการณ์ของน้ำและไฟ ความลึกลับของการมีปฏิสัมพันธ์ของพวกเขา ภาพที่เปลี่ยนแปลงนี้ช่างน่าหลงใหล เมื่อกาต้มน้ำเดือด มันก็เริ่มพูด” ทาลลินน์ อดามอฟสกายา
วันนี้เราจะดูกระบวนการนี้จากมุมมองทางกายภาพและพยายามค้นหาคำตอบของความลึกลับมากมายที่มาพร้อมกับปรากฏการณ์นี้ หัวข้อบทเรียนคือ "การเดือด" ความร้อนจำเพาะของการกลายเป็นไอและการควบแน่น”
นักเรียนเขียนหัวข้อของบทเรียนลงในสมุดบันทึก
ครู:เพื่อศึกษาการต้มเราจะทำการทดลอง วางขวดที่มีน้ำประปาไว้บนตะเกียงแอลกอฮอล์ มาวัดอุณหภูมิเริ่มต้นของน้ำด้วยเทอร์โมมิเตอร์กันดีกว่า
3. การอัพเดตความรู้
ครู: ขณะที่น้ำร้อนขึ้น ให้จำไว้ว่าเรียกว่าการระเหย
นักเรียน: การกลายเป็นไอเป็นปรากฏการณ์การเปลี่ยนของเหลวให้เป็นไอ
ครู: การกลายเป็นไอมี 2 วิธีอะไรบ้าง?
นักเรียน: การระเหยและการเดือด
ครู: ปรากฏการณ์ใดที่เรียกว่าการระเหย?
นักเรียน: การก่อตัวของไอที่เกิดขึ้นจากพื้นผิวของของเหลวเรียกว่าการระเหย
ครู: อธิบายกลไกการระเหยจากมุมมองของโมเลกุล
นักเรียน: วัตถุทั้งหมดประกอบด้วยโมเลกุลที่เคลื่อนที่อย่างต่อเนื่องและวุ่นวายด้วยความเร็วที่แตกต่างกัน หากโมเลกุล "เร็ว" ไปสิ้นสุดที่พื้นผิวของของเหลว ก็สามารถเอาชนะแรงดึงดูดของโมเลกุลข้างเคียงและลอยออกจากของเหลวได้ โมเลกุลทั้งหมดที่ปล่อยออกมาจะเกิดเป็นไอน้ำ
ครู: สารมีอุณหภูมิคงที่เมื่อเริ่มกระบวนการระเหยหรือไม่?
นักเรียน: สารไม่มีอุณหภูมิดังกล่าว การระเหยเกิดขึ้นที่อุณหภูมิใดๆ เนื่องจากโมเลกุลเคลื่อนที่ที่อุณหภูมิใดๆ
ครู: อะไรเป็นตัวกำหนดอัตราการระเหยของของเหลว?
นักเรียน: จากชนิดของสาร อุณหภูมิ พื้นที่ผิว และการเคลื่อนตัวของอากาศเหนือพื้นผิวของของเหลว
ครู: เหตุใดการระเหยจึงเกิดขึ้นเร็วขึ้นเมื่อมากขึ้น อุณหภูมิสูงของเหลว?
นักเรียน: ยิ่งอุณหภูมิสูงความเร็วของโมเลกุลก็จะยิ่งมากขึ้น
ครู: อัตราการระเหยขึ้นอยู่กับพื้นที่ผิวของของเหลวอย่างไร?
นักเรียน: ยิ่งพื้นที่ผิวมีขนาดใหญ่ โมเลกุลก็จะหลุดออกจากของเหลวได้มากขึ้นเท่านั้น
ครู: เหตุใดการระเหยจึงเกิดขึ้นเร็วขึ้นเมื่ออากาศเคลื่อนที่?
นักเรียน: โมเลกุลที่ระเหยไม่สามารถกลับคืนสู่ของเหลวได้
ครู: การควบแน่นของไอน้ำคืออะไร?
นักเรียน: การควบแน่นเป็นปรากฏการณ์การเปลี่ยนไอให้เป็นของเหลว
ครู: การควบแน่นของไอน้ำเกิดขึ้นภายใต้สภาวะใดบ้าง
นักเรียน: เมื่อไอระเหยอิ่มตัว กล่าวคือ ในสภาวะสมดุลไดนามิกกับของเหลว
4. ศึกษาเนื้อหาใหม่
ครู: กลับมาที่การทดลองของเรากันดีกว่า และวัดอุณหภูมิของน้ำ ตอนนี้คุณกำลังสังเกตอะไรอยู่?
นักเรียน: ฟองอากาศปรากฏขึ้นที่ด้านล่างและผนังของถัง (สไลด์ 3)
ครู: ทำไมฟองอากาศจึงปรากฏที่ด้านล่างและผนังของถัง?
นักเรียน: มีอากาศละลายในน้ำอยู่เสมอ เมื่อถูกความร้อน ฟองอากาศจะขยายตัวและมองเห็นได้
ครู: ทำไมฟองอากาศจึงเริ่มมีปริมาตรเพิ่มขึ้น?
นักเรียน: เพราะน้ำเริ่มระเหยภายในฟองเหล่านี้
ครู: แรงอะไรกระทำต่อฟอง?
นักเรียน: แรงโน้มถ่วงและแรงอาร์คิมีดีน
ครู: พวกเขามีทิศทางอะไร?
นักเรียน: แรงโน้มถ่วงมุ่งลง และแรงของอาร์คิมิดีสมุ่งขึ้น (สไลด์ 4)
ครู: เมื่อใดที่ฟองอากาศจะแตกออกจากด้านล่างและผนังของภาชนะและเริ่มเคลื่อนตัวขึ้นด้านบน
นักเรียน: ฟองอากาศจะหลุดออกมาเมื่อพลังอาร์คิมีดีนเกิดขึ้น มีพลังมากขึ้นแรงโน้มถ่วง.
ครู: มาวัดอุณหภูมิน้ำกันเถอะ ตอนนี้คุณได้ยินเสียงที่มีลักษณะเฉพาะ ให้เราอธิบายปรากฏการณ์นี้ หากปริมาตรของฟองมีขนาดใหญ่เพียงพอ แสดงว่าฟองนั้นอยู่ภายใต้อิทธิพล
พลังของอาร์คิมีดีสเริ่มเพิ่มสูงขึ้น เนื่องจากของเหลวถูกให้ความร้อนโดยการพาความร้อนอุณหภูมิ ชั้นล่างอุณหภูมิมากขึ้น ชั้นบนน้ำ. เมื่อฟองเข้าสู่ชั้นน้ำด้านบนซึ่งมีความร้อนน้อยกว่า ไอน้ำที่อยู่ภายในจะควบแน่นและปริมาตรของฟองจะลดลง ฟองจะยุบ (สไลด์ 5) เราได้ยินเสียงที่เกี่ยวข้องกับกระบวนการนี้ก่อนที่จะเดือด ที่อุณหภูมิหนึ่งนั่นคือเมื่อของเหลวทั้งหมดได้รับความร้อนเนื่องจากการพาความร้อนเมื่อเข้าใกล้พื้นผิวปริมาตรของฟองอากาศจะเพิ่มขึ้นอย่างรวดเร็วเนื่องจากความดันภายในฟองจะเท่ากับความดันภายนอก (ของบรรยากาศ และคอลัมน์ของเหลว) ฟองสบู่แตกบนพื้นผิวและมีไอน้ำจำนวนมากก่อตัวอยู่เหนือของเหลว น้ำกำลังเดือด
ตอนนี้เราจะวัดอุณหภูมิของน้ำเดือด น้ำเดือดที่อุณหภูมิ 100 o C
ครู: ดังนั้น สภาวะการเดือด: ความดันภายในฟองเท่ากับความดันภายนอกและสัญญาณของการเดือด:
ฟองอากาศจำนวนมากแตกออกมาบนพื้นผิว
ไอน้ำมากมาย
เดือดอะไร?
นักเรียน: การเดือดคือการก่อตัวของไอที่เกิดขึ้นในปริมาตรของของเหลวทั้งหมดที่อุณหภูมิที่กำหนด
ครู: มาเขียนคำจำกัดความของการเดือดกันดีกว่า (สไลด์ 6)
การเดือดคือการกลายเป็นไออย่างเข้มข้นที่เกิดขึ้นทั่วทั้งปริมาตรของของเหลวที่อุณหภูมิที่กำหนด
ครู: อุณหภูมิใดเรียกว่าจุดเดือด?
นักเรียน: อุณหภูมิที่ของเหลวเดือดเรียกว่าจุดเดือด
ครู: คุณคิดว่าอุณหภูมิจะเปลี่ยนแปลงในระหว่างกระบวนการต้มหรือไม่?
นักเรียน: ฉันคิดว่ามันจะไม่เปลี่ยนแปลง (สไลด์ 7)
ครู: มาวัดอุณหภูมิน้ำเดือดกันอีกครั้ง อุณหภูมิไม่เปลี่ยนแปลง แต่ตะเกียงแอลกอฮอล์ยังคงทำงานและปล่อยพลังงานต่อไป พลังงานนี้ถูกใช้ไปกับอะไรหากไม่มีอุณหภูมิเพิ่มขึ้นอีก?
นักเรียน: มันถูกใช้ไปกับการก่อตัวของฟองไอน้ำ
ครู: ดูตารางหน้า 45 ค้นหาจุดเดือดของน้ำ
นักเรียน: จุดเดือดของน้ำคือ 100 o C
ครู: ของเหลวชนิดใดมีจุดเดือดเท่ากัน?
นักเรียน: น้ำนม.
ครู: จุดเดือดของอีเทอร์และแอลกอฮอล์คือเท่าไร?
นักเรียน: อีเธอร์เดือดที่ 35 o C แอลกอฮอล์ - ที่ 78 o C
ครู: สารบางชนิดซึ่งภายใต้สภาวะปกติเป็นก๊าซเมื่อเย็นเพียงพอแล้วจะกลายเป็นของเหลวที่เดือดที่อุณหภูมิต่ำมาก สารใดต่อไปนี้อยู่ในตาราง?
นักเรียน: เหล่านี้คือไฮโดรเจนและออกซิเจน ไฮโดรเจนเหลวเดือดที่ -253 o C และออกซิเจนเดือดที่ -183 o C
ครู: ตอนนี้เราจะชมวิดีโอ “การต้มไนโตรเจน” (สไลด์ 8)
ครู: มีสารหลายชนิดในตารางที่เป็นของแข็งภายใต้สภาวะปกติ หากคุณละลายพวกมันในสถานะของเหลวพวกมันจะเดือดที่อุณหภูมิสูงมาก ยกตัวอย่าง.
นักเรียน: เช่น ทองแดงเหลวเดือดที่ 2567 o C และเหล็กเดือดที่ 2750 o C
ครู: คุณใส่ใจกับข้อมูลที่ระบุในวงเล็บในชื่อตารางนี้หรือไม่?
นักเรียน: จุดเดือดของสารบางชนิดที่ความดันบรรยากาศปกติ
ครู: ทำไมคุณถึงคิดว่าเงื่อนไขนี้ถูกระบุ?
นักเรียน: เพราะจุดเดือดขึ้นอยู่กับแรงดันภายนอก
ครู: ลองศึกษาการขึ้นอยู่กับอุณหภูมิจุดเดือดกับความดันภายนอก
การสาธิต: ยกขวดที่มีของเหลวเดือดออกจากตะเกียงแอลกอฮอล์ แล้วปิดด้วยจุกที่มีหลอดไฟเสียบอยู่ เมื่อคุณกดหัวหลอด น้ำเดือดในขวดจะหยุดลง ทำไม
นักเรียน: เมื่อเรากดหัวขวด เราได้เพิ่มความดันในขวด และสภาวะการเดือดก็ถูกละเมิด
ครู: ดังนั้น เราได้แสดงให้เห็นว่าเมื่อความดันเพิ่มขึ้น จุดเดือดจะเพิ่มขึ้น แม่บ้านหลายคนใช้กระทะในการปรุงอาหาร - หม้ออัดแรงดันซึ่งมีข้อดีมากกว่ากระทะธรรมดาหลายประการ กระบวนการปรุงอาหารในหม้ออัดแรงดันเกิดขึ้นที่อุณหภูมิ 120 o C และความดัน 200 kPa ดังนั้นเวลาในการปรุงอาหารจึงลดลงอย่างมาก (สไลด์ 9)
ครู: จำไว้ว่ามันเปลี่ยนไปอย่างไร ความดันบรรยากาศด้วยความสูงเหนือระดับน้ำทะเลที่เพิ่มขึ้น?
นักเรียน: ความดันบรรยากาศลดลง
ครู: จุดเดือดของน้ำเวลาขึ้นเขาเปลี่ยนแปลงอย่างไร?
นักเรียน: มันจะลดลง (สไลด์ 10)
ครู: ถูกต้องอย่างแน่นอน. ยกตัวอย่างมากที่สุด ภูเขาสูงจอมลุงมาในเทือกเขาหิมาลัยซึ่งมีความสูง 8848 ม. น้ำจะเดือดที่อุณหภูมิประมาณ 70 o C เป็นไปไม่ได้เลยที่จะปรุงเนื้อสัตว์ในน้ำเดือดเช่นนี้
คุณคิดว่าเป็นไปได้ไหมที่จะทำให้น้ำเดือดที่อุณหภูมิห้อง เพราะเหตุใด
สาธิต: แก้วด้วย น้ำเย็นวางไว้ใต้ระฆังแก้ว ใช้ปั๊ม Komovsky เพื่อสูบลมออก เมื่อความดันในแก้วลดลง เราจะสังเกตขั้นตอนการเดือดของของเหลวในขณะที่อุณหภูมิยังคงต่ำ
ครู: ได้ข้อสรุปอะไรจากการทดลองบ้าง?
นักเรียน: จุดเดือดของของเหลวขึ้นอยู่กับความดัน
ครู: เรามาทำความรู้จักกับกระบวนการต้ม คุณคิดว่าต้องใช้ความร้อนในปริมาณเท่ากันในการต้มของเหลวต่าง ๆ ที่มีมวลเท่ากันที่จุดเดือดหรือไม่ เพราะเหตุใด
นักเรียน: ฉันคิดว่าต้องใช้ความร้อนในปริมาณที่แตกต่างกัน
ครู: ถูกต้อง (สไลด์ 11) ในแผนภาพ เราจะเห็นว่าต้องใช้ความร้อนในปริมาณที่แตกต่างกันในการเปลี่ยนของเหลวต่างๆ ให้เป็นไอ ปริมาณความร้อนนี้มีลักษณะเป็นปริมาณทางกายภาพที่เรียกว่าความร้อนจำเพาะของการกลายเป็นไอ ปริมาณนี้แสดงด้วยตัวอักษร L โดยมีหน่วย SI คือ J/kg ความร้อนจำเพาะของการกลายเป็นไอคือปริมาณทางกายภาพที่แสดงปริมาณความร้อนที่จำเป็นในการเปลี่ยนของเหลวที่มีน้ำหนัก 1 กิโลกรัมให้เป็นไอน้ำที่จุดเดือด ลองดูตารางในหน้า 49 เช่น ความร้อนจำเพาะของการกลายเป็นไอของน้ำคือ 2.3*10 6 J/kg ซึ่งหมายความว่าในการแปลงน้ำ 1 กิโลกรัมเป็นไอน้ำที่จุดเดือด คุณจะต้องใช้พลังงาน 2.3 * 10 6 J ความร้อนจำเพาะของการระเหยของแอลกอฮอล์เป็นเท่าใด
นักเรียน: ความร้อนจำเพาะของการกลายเป็นไอของแอลกอฮอล์ 0.9*10 6 J/kg.
ครู: ตัวเลขนี้หมายถึงอะไร?
นักเรียน: ซึ่งหมายความว่าในการแปลงแอลกอฮอล์ 1 กิโลกรัมเป็นไอน้ำที่จุดเดือด คุณจะต้องใช้พลังงาน 0.9 * 10 6 J
ครู: ดังนั้น ณ จุดเดือด พลังงานภายในของสารในสถานะไอจึงมากกว่าพลังงานภายในของสารที่มีมวลเท่ากันในสถานะของเหลว ด้วยเหตุนี้การเผาด้วยไอน้ำที่อุณหภูมิ 100 o C จึงเป็นอันตรายมากกว่าการเผาด้วยน้ำเดือด (สไลด์ 12)
ตอนนี้ตอบคำถาม: ถ้าคุณถอดฝาออกจากกาต้มน้ำเดือดคุณเห็นอะไรบนนั้น?
นักเรียน: เราจะเห็นหยดน้ำตรงนั้น
ครู: คุณจะอธิบายรูปลักษณ์ของพวกเขายังไง?
นักเรียน: ไอน้ำที่สัมผัสกับฝาปิดควบแน่น (สไลด์ 13)
ครู: เมื่อไอน้ำควบแน่น พลังงานจะถูกปล่อยออกมา การทดลองแสดงให้เห็นว่าเมื่อไอน้ำควบแน่นจะปล่อยความร้อนออกมาในปริมาณเท่ากันกับที่ใช้ไปกับการก่อตัวของมัน สามารถใช้พลังงานที่ปล่อยออกมาระหว่างการควบแน่นของไอน้ำได้ ที่โรงไฟฟ้าพลังความร้อน น้ำจะถูกทำให้ร้อนด้วยไอน้ำที่ใช้หมดจากกังหัน จากนั้นนำไปใช้ในการทำความร้อนในอาคารและในสถานประกอบการบริการสาธารณะ เช่น อ่างอาบน้ำ ห้องซักรีด ฯลฯ
ในการคำนวณปริมาณความร้อนที่ต้องใช้ในการแปลงของเหลวที่มีมวลใดๆ ให้เป็นไอที่จุดเดือด คุณต้องคูณความร้อนจำเพาะของการกลายเป็นไอด้วยมวล ลองเขียนสูตร: Q = Lm ปริมาณความร้อนที่ไอน้ำของมวลใดๆ ปล่อยออกมาเมื่อควบแน่นที่จุดเดือดจะถูกกำหนดโดยสูตรเดียวกัน
5. การรวมบัญชี
ครู: ตอนนี้คุณรู้วิธีการกลายเป็นไอสองวิธีแล้ว: การระเหยและการเดือด ใครสามารถบอกได้ว่ากระบวนการเหล่านี้แตกต่างกันอย่างไร
นักเรียน: การระเหยเกิดขึ้นจากพื้นผิวของของเหลว และการเดือดเกิดขึ้นตลอดปริมาตรของของเหลวทั้งหมด
นักเรียน: การระเหยเกิดขึ้นที่อุณหภูมิใด ๆ และการเดือดจะเกิดขึ้นที่อุณหภูมิหนึ่ง ของเหลวแต่ละชนิดมีจุดเดือดของตัวเอง
นักเรียน: เมื่อระเหย อุณหภูมิของของเหลวจะลดลงแต่เมื่อเดือดจะไม่เปลี่ยนแปลง
ครู: คุณคิดว่าน้ำเดือดร้อนกว่าที่ไหน: ที่ระดับน้ำทะเล บนภูเขา หรือในเหมืองลึก
นักเรียน: ฉันคิดว่าน้ำในเหมืองลึกจะร้อนกว่าเพราะความดันบรรยากาศที่ระดับความลึกจะสูงขึ้น น้ำจึงจะเดือดที่อุณหภูมิสูงขึ้น
ครู: สามารถใช้สูตรใดในการคำนวณปริมาณความร้อนที่ใช้ไปกับการก่อตัวของไอน้ำหรือปล่อยออกมาระหว่างการควบแน่นของไอน้ำ
ครู: ลองคำนวณปริมาณความร้อนด้วยวาจาในกรณีต่อไปนี้ (สไลด์ 15):
นักเรียน: สำหรับอีเทอร์ Q = 2*10 6 J สำหรับแอลกอฮอล์ – 9*10 6 J สำหรับน้ำ – 4.6*10 6 J
ครู: กราฟแสดงกระบวนการให้ความร้อนและการเดือดของของเหลวสองชนิดที่มีมวลเท่ากัน (สไลด์ 16) ใช้ตารางในหน้า 45 เพื่อพิจารณาว่ากราฟถูกสร้างขึ้นสำหรับสารใด
นักเรียน: อันบนสำหรับน้ำ อันล่างสำหรับแอลกอฮอล์ เนื่องจากจุดเดือดของน้ำคือ 100 o C และจุดเดือดของแอลกอฮอล์คือ 78 o C
ครู: อุณหภูมิเริ่มต้นของของเหลวคือเท่าไร?
นักเรียน: อุณหภูมิเริ่มต้นของของเหลวทั้งสองคือ 20? C
ครู: ตั้งชื่อส่วนของกราฟที่สอดคล้องกับการให้ความร้อนของของเหลว
นักเรียน: AB สำหรับแอลกอฮอล์ และ AD สำหรับน้ำ
ครู: ตั้งชื่อส่วนของกราฟที่สอดคล้องกับการเดือดของของเหลว
นักเรียน: BC สำหรับแอลกอฮอล์ และ DE สำหรับน้ำ
6. สรุปบทเรียน
ครู: เปิดสมุดบันทึกของคุณและจดการบ้านของคุณ: ย่อหน้า 18, 20 แบบฝึกหัด 10(4) (สไลด์ 17)
สำหรับผู้ที่สนใจงานทดลองดังต่อไปนี้
ใช้หม้อน้ำขนาดใหญ่ วางกระทะน้ำใบเล็กลงไปเพื่อให้ลอยน้ำโดยไม่แตะก้นกระทะใบใหญ่ วางไว้บนเตาแล้วเริ่มทำความร้อน จะเกิดอะไรขึ้นกับน้ำในหม้อใบเล็กเมื่อต้มในหม้อใบใหญ่? ทำไม ใส่เกลือหนึ่งช้อนโต๊ะลงในกระทะขนาดใหญ่ จะเกิดอะไรขึ้นกับน้ำในกระทะใบเล็กหลังจากนี้? อธิบายปรากฏการณ์ที่สังเกตได้ คุณจะพูดอะไรเกี่ยวกับจุดเดือดของน้ำเกลือได้บ้าง?
7. การสะท้อนกลับ.
ครู: บทเรียนของเรากำลังจะจบลง ฉันอยากรู้ว่าคุณจะจากไปในอารมณ์ไหน บนโต๊ะคุณมีสติกเกอร์สีสามสีที่สะท้อนถึงอารมณ์ต่อไปนี้: สีเขียว - ฉันชอบบทเรียนมาก สีฟ้า - ฉันสนใจ สีแดง - ฉันเบื่อ เมื่อออกเดินทาง ให้ติดสติกเกอร์ที่แสดงอารมณ์ของคุณไว้บนกระดาน (สไลด์ 18)
บทเรียนจบลงแล้ว ขอบคุณสำหรับความสนใจของคุณ!
แหล่งที่มา
- เอ.วี. เพอริชกิน ฟิสิกส์. ชั้นประถมศึกษาปีที่ 8 - ม.; อีแร้ง
- อี.เอ็ม. กุตนิค, อี, วี. Rybakova, E.V. ชาโรนินา. วัสดุระเบียบวิธีสำหรับครู ฟิสิกส์. ชั้นประถมศึกษาปีที่ 8 - ม.; อีแร้ง
- แอลเอ โกเรฟ. การทดลองที่สนุกสนานในวิชาฟิสิกส์ – ม.;
- การศึกษา
- คอลเลกชันทรัพยากรการศึกษาดิจิทัลแบบครบวงจร:
- วีดิทัศน์เรื่อง “การต้มไนโตรเจน”
ภาพวาดจากการนำเสนอแบบแฟลช
ในบทนี้ เราจะให้ความสนใจกับการระเหยประเภทนี้ เช่น การเดือด อภิปรายการความแตกต่างจากขั้นตอนการระเหยที่กล่าวถึงก่อนหน้านี้ แนะนำค่าต่างๆ เช่น อุณหภูมิจุดเดือด และอภิปรายว่าขึ้นอยู่กับอะไร ในตอนท้ายของบทเรียน เราจะแนะนำปริมาณที่สำคัญมากซึ่งอธิบายกระบวนการของการกลายเป็นไอ - ความร้อนจำเพาะของการกลายเป็นไอและการควบแน่น
หัวข้อ: สถานะรวมของสสาร
บทเรียน: การเดือด ความร้อนจำเพาะของการกลายเป็นไอและการควบแน่น
ในบทเรียนที่แล้ว เราได้ศึกษาการก่อตัวของไอประเภทหนึ่งแล้ว ซึ่งก็คือ การระเหย และได้เน้นย้ำถึงคุณสมบัติของกระบวนการนี้ วันนี้เราจะมาพูดถึงการกลายเป็นไอประเภทนี้ กระบวนการเดือด และแนะนำค่าที่แสดงคุณลักษณะเชิงตัวเลขของกระบวนการกลายเป็นไอ - ความร้อนจำเพาะของการกลายเป็นไอและการควบแน่นคำนิยาม.เดือด
ลองเปรียบเทียบการกลายเป็นไอทั้งสองประเภทด้วยกัน กระบวนการเดือดมีความเข้มข้นมากกว่ากระบวนการระเหย นอกจากนี้ ดังที่เราจำได้ว่า กระบวนการระเหยเกิดขึ้นที่อุณหภูมิใดๆ ที่สูงกว่าจุดหลอมเหลว และกระบวนการเดือดอย่างเคร่งครัดที่อุณหภูมิที่กำหนด ซึ่งจะแตกต่างกันไปในแต่ละสารและเรียกว่าจุดเดือด ควรสังเกตด้วยว่าการระเหยเกิดขึ้นเฉพาะกับ พื้นผิวฟรีของเหลวเช่น จากพื้นที่ที่แยกออกจากก๊าซโดยรอบและการเดือด - จากปริมาตรทั้งหมดในคราวเดียว
มาดูขั้นตอนการต้มกันดีกว่า ลองจินตนาการถึงสถานการณ์ที่พวกเราหลายคนต้องเผชิญซ้ำแล้วซ้ำเล่า - การทำความร้อนและต้มน้ำในภาชนะบางประเภท เช่น กระทะ ในระหว่างการทำความร้อน ความร้อนจำนวนหนึ่งจะถูกถ่ายโอนไปยังน้ำ ซึ่งจะนำไปสู่การเพิ่มขึ้นของพลังงานภายในและการเพิ่มขึ้นของการเคลื่อนไหวของโมเลกุล กระบวนการนี้จะดำเนินต่อไปจนถึงระยะหนึ่งจนกระทั่งพลังงานการเคลื่อนที่ของโมเลกุลเพียงพอที่จะเริ่มเดือด
น้ำประกอบด้วยก๊าซละลาย (หรือสิ่งเจือปนอื่น ๆ) ที่ถูกปล่อยออกมาในโครงสร้าง ซึ่งนำไปสู่สิ่งที่เรียกว่าศูนย์การกลายเป็นไอ นั่นคืออยู่ในศูนย์เหล่านี้ที่ไอน้ำเริ่มถูกปล่อยออกมาและฟองจะก่อตัวขึ้นทั่วทั้งปริมาตรน้ำซึ่งสังเกตได้ในระหว่างการเดือด สิ่งสำคัญคือต้องเข้าใจว่าฟองเหล่านี้ไม่มีอากาศ แต่มีไอน้ำเกิดขึ้นระหว่างกระบวนการเดือด หลังจากการก่อตัวของฟองอากาศ ปริมาณไอน้ำในนั้นจะเพิ่มขึ้น และเริ่มมีขนาดเพิ่มขึ้น บ่อยครั้งที่ฟองสบู่ก่อตัวขึ้นใกล้ผนังของภาชนะและไม่ลอยขึ้นสู่ผิวน้ำในทันที ประการแรก การเพิ่มขนาด พวกมันได้รับอิทธิพลจากพลังที่เพิ่มขึ้นของอาร์คิมิดีส จากนั้นพวกมันก็แยกตัวออกจากกำแพงและขึ้นสู่ผิวน้ำ โดยพวกมันจะระเบิดและปล่อยไอน้ำบางส่วนออกมา
เป็นที่น่าสังเกตว่าไม่ใช่ว่าฟองไอน้ำทั้งหมดจะไปถึงผิวน้ำในทันที ในช่วงเริ่มต้นของกระบวนการเดือด น้ำยังไม่ได้รับความร้อนเท่ากัน และชั้นล่างซึ่งใกล้กับกระบวนการถ่ายเทความร้อนเกิดขึ้นโดยตรงจะร้อนกว่าชั้นบนด้วยซ้ำ แม้จะคำนึงถึงกระบวนการพาความร้อนด้วยซ้ำ สิ่งนี้นำไปสู่ความจริงที่ว่าฟองไอน้ำที่เพิ่มขึ้นจากด้านล่างยุบตัวลงเนื่องจากปรากฏการณ์แรงตึงผิว ก่อนที่จะถึงพื้นผิวอิสระของน้ำ ในกรณีนี้ไอน้ำที่อยู่ภายในฟองสบู่จะผ่านลงไปในน้ำซึ่งจะให้ความร้อนเพิ่มเติมและเร่งกระบวนการให้ความร้อนสม่ำเสมอของน้ำตลอดทั้งปริมาตร ผลก็คือ เมื่อน้ำอุ่นขึ้นเกือบเท่าๆ กัน ฟองไอน้ำเกือบทั้งหมดจะเริ่มขึ้นถึงผิวน้ำ และกระบวนการสร้างไอน้ำเข้มข้นก็เริ่มต้นขึ้น
สิ่งสำคัญคือต้องเน้นความจริงที่ว่าอุณหภูมิที่กระบวนการเดือดเกิดขึ้นยังคงไม่เปลี่ยนแปลงแม้ว่าความเข้มข้นของความร้อนที่จ่ายให้กับของเหลวจะเพิ่มขึ้นก็ตาม ด้วยคำพูดง่ายๆหากในระหว่างกระบวนการเดือดคุณเติมแก๊สลงในเตาที่ให้ความร้อนกับกระทะ สิ่งนี้จะนำไปสู่การเพิ่มความเข้มข้นของการเดือดเท่านั้นและไม่ทำให้อุณหภูมิของของเหลวเพิ่มขึ้น หากเราเจาะลึกกระบวนการเดือดอย่างจริงจังมากขึ้นก็น่าสังเกตว่าบริเวณนั้นปรากฏในน้ำซึ่งสามารถทำให้ร้อนเกินไปเหนือจุดเดือดได้ แต่ตามกฎแล้วปริมาณของความร้อนสูงเกินไปดังกล่าวจะต้องไม่เกินหนึ่งหรือสองสามองศา และมีปริมาตรของเหลวรวมไม่มีนัยสำคัญ จุดเดือดของน้ำที่ ความดันปกติคือ 100°C
ในระหว่างกระบวนการต้มน้ำคุณสามารถสังเกตเห็นว่ามันมาพร้อมกับเสียงลักษณะของสิ่งที่เรียกว่าเดือด เสียงเหล่านี้เกิดขึ้นอย่างแม่นยำเนื่องจากกระบวนการยุบฟองไอน้ำที่อธิบายไว้
กระบวนการเดือดของของเหลวอื่นๆ ดำเนินไปในลักษณะเดียวกับการต้มน้ำ ความแตกต่างที่สำคัญในกระบวนการเหล่านี้คืออุณหภูมิจุดเดือดที่แตกต่างกันของสาร ซึ่งค่าแบบตารางจะวัดที่ความดันบรรยากาศปกติแล้ว เราระบุค่าหลักของอุณหภูมิเหล่านี้ในตาราง
ข้อเท็จจริงที่น่าสนใจคือจุดเดือดของของเหลวขึ้นอยู่กับค่าของความดันบรรยากาศซึ่งเป็นเหตุผลที่เราระบุว่าค่าทั้งหมดในตารางจะได้รับที่ความดันบรรยากาศปกติ เมื่อความดันอากาศเพิ่มขึ้น จุดเดือดของของเหลวก็จะเพิ่มขึ้นเช่นกัน เมื่อลดลง ในทางกลับกันก็จะลดลง
ขึ้นอยู่กับอุณหภูมิเดือดกับความดันนี้ สิ่งแวดล้อมตามหลักการทำงานของเครื่องใช้ในครัวที่มีชื่อเสียงเช่นหม้ออัดแรงดัน (รูปที่ 2) เป็นกระทะที่มีฝาปิดแน่นซึ่งในระหว่างกระบวนการนึ่งน้ำความดันอากาศที่มีไอน้ำสูงถึง 2 ความดันบรรยากาศซึ่งทำให้จุดเดือดของน้ำเพิ่มขึ้นเป็น . ด้วยเหตุนี้น้ำและอาหารในนั้นจึงมีโอกาสให้ความร้อนสูงถึงอุณหภูมิที่สูงกว่าปกติ () และกระบวนการปรุงอาหารก็เร่งขึ้น ด้วยเหตุนี้อุปกรณ์จึงได้ชื่อมา

ข้าว. 2. หม้ออัดแรงดัน ()
สถานการณ์ที่มีจุดเดือดของของเหลวลดลงและความดันบรรยากาศลดลงก็มีตัวอย่างจากชีวิตเช่นกัน แต่ไม่ใช่ทุกวันสำหรับหลาย ๆ คนอีกต่อไป ตัวอย่างนี้ใช้กับการเดินทางของนักปีนเขาในพื้นที่ภูเขาสูง ปรากฎว่าในพื้นที่ที่ตั้งอยู่ที่ระดับความสูง 3,000-5,000 ม. จุดเดือดของน้ำเนื่องจากความดันบรรยากาศลดลงจะลดลงเหลือค่าที่ต่ำกว่าซึ่งนำไปสู่ความยากลำบากในการเตรียมอาหารขณะเดินป่าเพราะ เพื่อการบำบัดความร้อนอย่างมีประสิทธิภาพ สินค้าในกรณีนี้สำคัญ เวลานานขึ้นกว่าด้วย สภาวะปกติ- ที่ระดับความสูงประมาณ 7,000 ม. จุดเดือดของน้ำถึง ซึ่งทำให้ไม่สามารถปรุงผลิตภัณฑ์จำนวนมากในสภาวะดังกล่าวได้
เทคโนโลยีบางอย่างในการแยกสารขึ้นอยู่กับข้อเท็จจริงที่ว่าจุดเดือดของสารต่างๆ ต่างกัน ตัวอย่างเช่น หากเราพิจารณาน้ำมันให้ความร้อนซึ่งเป็นของเหลวเชิงซ้อนที่ประกอบด้วยส่วนประกอบหลายอย่าง ในระหว่างกระบวนการเดือด ก็สามารถแบ่งออกเป็นสารต่างๆ ได้หลายชนิด ในกรณีนี้เนื่องจากจุดเดือดของน้ำมันก๊าด น้ำมันเบนซิน แนฟทา และน้ำมันเชื้อเพลิงแตกต่างกัน จึงสามารถแยกออกจากกันโดยการกลายเป็นไอและการควบแน่นที่อุณหภูมิต่างกัน กระบวนการนี้มักเรียกว่าการแยกส่วน (รูปที่ 3)

ข้าว. 3 การแยกน้ำมันออกเป็นเศษส่วน ()
เช่นเดียวกับกระบวนการทางกายภาพอื่นๆ การเดือดจะต้องถูกกำหนดลักษณะโดยใช้ค่าตัวเลข ค่านี้เรียกว่าความร้อนจำเพาะของการกลายเป็นไอ
เพื่อให้เกิดความเข้าใจ ความหมายทางกายภาพค่านี้พิจารณาตัวอย่างต่อไปนี้: นำน้ำ 1 กิโลกรัมไปที่จุดเดือดจากนั้นวัดว่าต้องใช้ความร้อนเท่าใดในการระเหยน้ำนี้ให้หมด (โดยไม่คำนึงถึงการสูญเสียความร้อน) - ค่านี้จะเท่ากับค่าเฉพาะ ความร้อนของการระเหยของน้ำ สำหรับสารอื่น ค่าความร้อนนี้จะแตกต่างออกไปและจะเป็นความร้อนจำเพาะของการกลายเป็นไอของสารนี้
ความร้อนจำเพาะของการกลายเป็นไอกลายเป็นคุณลักษณะที่สำคัญมาก เทคโนโลยีที่ทันสมัยการผลิตโลหะ ปรากฎว่าในระหว่างการหลอมและการระเหยของเหล็กด้วยการควบแน่นและการแข็งตัวตามมานั้น โครงตาข่ายคริสตัลจะเกิดขึ้นพร้อมกับโครงสร้างที่ให้ความแข็งแรงสูงกว่าตัวอย่างดั้งเดิม
การกำหนด: ความร้อนจำเพาะของการกลายเป็นไอและการควบแน่น (บางครั้งแสดงแทน )
หน่วยวัด: .
ความร้อนจำเพาะของการกลายเป็นไอของสารถูกกำหนดโดยใช้การทดลองในห้องปฏิบัติการและค่าของสารพื้นฐานแสดงอยู่ในตารางที่เหมาะสม
|
สาร |
ความจุความร้อนจำเพาะ
ความร้อนจำเพาะคือปริมาณความร้อนในหน่วยจูลส์ (J) ที่ต้องใช้ในการเพิ่มอุณหภูมิของสาร ความจุความร้อนจำเพาะเป็นฟังก์ชันของอุณหภูมิ สำหรับก๊าซจำเป็นต้องแยกแยะความจุความร้อนจำเพาะที่ ความดันคงที่และด้วยปริมาตรคงที่
ความร้อนจำเพาะของฟิวชัน
ความร้อนจำเพาะของฟิวชัน แข็งคือปริมาณความร้อนในหน่วย J ที่ต้องใช้ในการแปลงสาร 1 กิโลกรัมจากของแข็งเป็นของเหลวที่จุดหลอมเหลว
ความร้อนแฝงของการกลายเป็นไอ
ความร้อนแฝงของการกลายเป็นไอของของเหลวคือปริมาณความร้อนใน J ที่ต้องใช้ในการระเหยของเหลว 1 กิโลกรัมที่จุดเดือด ความร้อนแฝงของการกลายเป็นไอจะขึ้นอยู่กับความดันเป็นอย่างมาก ตัวอย่าง: หากให้ความร้อนกับภาชนะที่บรรจุน้ำ 1 กิโลกรัม ที่อุณหภูมิ 100°C (ระดับน้ำทะเล) น้ำจะดูดซับความร้อนแฝง 1,023 กิโลจูล โดยไม่มีการเปลี่ยนแปลงใดๆ ในการอ่านค่าเทอร์โมมิเตอร์ อย่างไรก็ตามจะมีการเปลี่ยนแปลงสถานะการรวมตัวจากของเหลวเป็นไอ ความร้อนที่น้ำดูดซับเรียกว่าความร้อนแฝงของการกลายเป็นไอ
ไอน้ำจะคงไว้ 1,023 กิโลจูล เนื่องจากพลังงานนี้จำเป็นต่อการเปลี่ยนสถานะการรวมตัว
ในกระบวนการย้อนกลับ เมื่อนำความร้อนออกจากไอน้ำ 1 กิโลกรัมที่อุณหภูมิ 100°C (ที่ระดับน้ำทะเล) ไอน้ำจะปล่อยความร้อนออกมา 1,023 กิโลจูล โดยไม่ต้องเปลี่ยนการอ่านค่าเทอร์โมมิเตอร์ อย่างไรก็ตามจะมีการเปลี่ยนแปลงสถานะการรวมตัวจากไอเป็นของเหลว ความร้อนที่น้ำดูดซับเรียกว่าความร้อนแฝงของการควบแน่น
อุณหภูมิและความดัน

การวัดความร้อน
อุณหภูมิหรือความเข้มของความร้อนวัดด้วยเทอร์โมมิเตอร์ อุณหภูมิส่วนใหญ่ในคู่มือเล่มนี้แสดงเป็นองศาเซลเซียส (C) แต่บางครั้งก็ใช้องศาฟาเรนไฮต์ (F) ค่าอุณหภูมิบอกเราเพียงความเข้มของความร้อนหรือความร้อนที่ละเอียดอ่อน ไม่ใช่ปริมาณความร้อนที่แท้จริง อุณหภูมิที่สะดวกสบายสำหรับบุคคลอยู่ระหว่าง 21 ถึง 27°C ในช่วงอุณหภูมินี้บุคคลจะรู้สึกสบายที่สุด เมื่ออุณหภูมิใดๆ สูงกว่าหรือต่ำกว่าช่วงนี้ บุคคลจะรับรู้ว่าอุณหภูมินั้นอุ่นหรือเย็น ในทางวิทยาศาสตร์ มีแนวคิดเรื่อง "ศูนย์สัมบูรณ์" ซึ่งเป็นอุณหภูมิที่ความร้อนทั้งหมดถูกขับออกจากร่างกาย อุณหภูมิศูนย์สัมบูรณ์ถูกกำหนดให้เป็น –273°C สารใดๆ ที่อุณหภูมิสูงกว่าศูนย์สัมบูรณ์จะมีความร้อนอยู่จำนวนหนึ่ง เพื่อให้เข้าใจพื้นฐานของเครื่องปรับอากาศ จำเป็นต้องเข้าใจความสัมพันธ์ระหว่างความดัน อุณหภูมิ และสถานะของสสารด้วย โลกของเราถูกล้อมรอบด้วยอากาศ หรืออีกนัยหนึ่งคือก๊าซ แรงดันในแก๊สจะถูกส่งอย่างเท่าเทียมกันในทุกทิศทาง ก๊าซรอบตัวเราประกอบด้วยออกซิเจน 21% และไนโตรเจน 78%ส่วนที่เหลืออีก 1% ถูกครอบครองโดยก๊าซหายากอื่นๆ การรวมกันของก๊าซนี้เรียกว่าบรรยากาศ ทอดยาวไปหลายร้อยกิโลเมตรเหนือ
พื้นผิวโลก
และถูกยึดไว้ด้วยแรงโน้มถ่วง ที่ระดับน้ำทะเล ความดันบรรยากาศคือ 1.0 บาร์ และจุดเดือดของน้ำคือ 100°C
การเรียนรู้และการรวมเนื้อหาทางทฤษฎีในหัวข้อหลักสูตรอุณหพลศาสตร์ "ไอน้ำ" รวมถึงการเรียนรู้วิธีการทดลองและการประมวลผลข้อมูลที่ได้รับ ทำความคุ้นเคยกับตาราง "คุณสมบัติทางอุณหพลศาสตร์ของน้ำและไอน้ำ"
1. ศึกษาแผนภาพของการติดตั้งทดลอง เปิดเครื่องและนำไปไว้ที่ระบบการระบายความร้อนแบบคงที่ที่กำหนด
2. ดำเนินการทดลองตามคำแนะนำด้านระเบียบวิธีกรอกตารางที่ 1
3. กำหนดความร้อนจำเพาะที่ใช้กับการระเหยของน้ำในการทดลอง
4. สำหรับกระบวนการไอโซบาริกของการกลายเป็นไอ ให้กำหนดค่าตารางของพารามิเตอร์ของน้ำบนเส้นอิ่มตัวและไอน้ำอิ่มตัวแบบแห้งตลอดจนความร้อนจำเพาะของการกลายเป็นไอ
5. คำนวณพลังงานภายในของของเหลวบนเส้นอิ่มตัวของไอสำหรับเงื่อนไขการทดลอง
6. คำนวณข้อผิดพลาดของค่าที่พบของความร้อนจำเพาะของการกลายเป็นไอซึ่งสัมพันธ์กับค่าในตาราง
7. บรรยายถึงกระบวนการที่เกิดขึ้นในภาชนะ Dewar ในแผนภาพ P-v และ T-s
8. สรุปผลการทำงาน
คำแนะนำด้านระเบียบวิธี
การเปลี่ยนผ่านของสารจากของเหลวไปเป็นสถานะก๊าซเรียกว่าการกลายเป็นไอ และการเปลี่ยนผ่านแบบย้อนกลับเรียกว่าการควบแน่น การต้มของเหลวเป็นกระบวนการของการกลายเป็นไอภายในของเหลวที่เกิดขึ้นที่อุณหภูมิที่กำหนดไว้อย่างเคร่งครัด t n, °C ซึ่งกำหนดโดยความดัน หากมีสถานะก๊าซและมีสถานะเป็นของเหลวของสารชนิดเดียวกัน จะเรียกว่าไอ เฟสก๊าซของระบบคือไอน้ำอิ่มตัวแห้ง และเฟสของเหลวเป็นของเหลวที่คงสถานะที่สอดคล้องกับการกลายเป็นไอ
ในระหว่างการกลายเป็นไอตามกระบวนการไอโซบาริก-ไอโซเทอร์มอล ตามกฎข้อที่หนึ่งของอุณหพลศาสตร์ ความร้อนจำเพาะของการเปลี่ยนเฟส (ความร้อนจำเพาะของการกลายเป็นไอ) r, J/kg
r = คุณ" - คุณ" + p (v" -v"), (1)
ร = ฉัน" - ฉัน" , (2)
คุณอยู่ที่ไหน", ฉัน", v" - ตามลำดับ พลังงานภายใน เอนทาลปี J/กก. และปริมาตรจำเพาะของไอน้ำอิ่มตัวแห้ง m 3 /กก.
u", i", v" - พลังงานภายในตามลำดับ, เอนทาลปี, J/kg และปริมาตรจำเพาะของของเหลวในสถานะอิ่มตัว m 3 /kg
ความดัน p, Pa ไม่ได้ทำเครื่องหมายด้วยดัชนีพิเศษเนื่องจากจะไม่เปลี่ยนแปลงระหว่างการเปลี่ยนเฟสทั้งหมดและเท่ากับความดันอิ่มตัว
ดังนั้นความร้อนจำเพาะของการกลายเป็นไอจึงรวมถึงการเปลี่ยนแปลงพลังงานภายในของสารและการทำงานของการเปลี่ยนแปลงปริมาตรระหว่างการเปลี่ยนเฟส
ความร้อนจำเพาะของการกลายเป็นไอมีความสัมพันธ์เชิงหน้าที่กับพารามิเตอร์สถานะ สำหรับสารส่วนใหญ่ที่ใช้ในทางปฏิบัติ คุณสมบัติของของเหลวและไอที่เส้นอิ่มตัวจะถูกกำหนดและทำเป็นตาราง ตารางเหล่านี้แสดงค่าของ p และ t บนเส้นอิ่มตัวและค่าที่สอดคล้องกันของปริมาณ v", v", i", i", r, s", s" พลังงานภายในของของเหลวบนเส้นอิ่มตัว u", J/kg และไอน้ำอิ่มตัวแห้ง u", J/kg จะถูกกำหนดตามสมการ
คุณ" = ฉัน" -pv" (3)
คุณ" = ฉัน" -pv" (4)
การตั้งค่าทดลอง
การวาดภาพ. แผนภาพการตั้งค่าการทดลอง
การตั้งค่าการทดลอง (รูป) ประกอบด้วยขวด Dewar 1 พร้อมเครื่องทำความร้อนไฟฟ้า 2 โดยเทน้ำกลั่นส่วนหนึ่งจากภาชนะ 3 ซึ่งควบคุมโดยวาล์ว 4 เข้าไป ไอน้ำที่เกิดขึ้นในคอนเดนเซอร์ 5 ซึ่งน้ำประปาไหลผ่านจะหมุนไป ให้เป็นของเหลว การไหลของน้ำถูกควบคุมโดยวาล์ว 7 ตามไฟควบคุม 8 คอนเดนเสทที่ได้จะถูกรวบรวมในกระบอกวัด 9 บนแผงควบคุมมี: สวิตช์ "เครือข่าย" 10, โวลต์มิเตอร์ 11, แอมมิเตอร์ 12, สวิตช์โหมด 13; 6 - ช่องทางแก้ว
วิธีการทดลอง
1. เปิดการติดตั้งโดยหมุนสวิตช์ 10 ไปที่ตำแหน่ง “1”
2. ตรวจสอบการเติมของภาชนะ Dewar 1 โดยการตั้งค่าสวิตช์โหมด 13 ไปที่ตำแหน่ง “การเติม” หากสัญญาณไฟสีเขียว “เรือเต็ม” สว่างขึ้น คุณสามารถเริ่มการทดลองได้ มิฉะนั้น ภาชนะจะเต็มไปด้วยน้ำกลั่น โดยวาล์ว 4 จะเปิดอยู่ หลังจากที่ไฟสัญญาณสีเขียวสว่างขึ้น ให้ปิดภาชนะให้แน่น
3. หมุนสวิตช์ 13 ไปที่ตำแหน่ง “ทำความร้อน”
4. โดยการหมุนปุ่มเปลี่ยนหม้อแปลงอัตโนมัติ 14 ให้ตั้งค่าแรงดันไฟฟ้าบนฮีตเตอร์ U, V (และกระแส I, A) ที่อาจารย์กำหนด
5. จ่ายน้ำหล่อเย็นให้กับคอนเดนเซอร์ 5 โดยเปิดวาล์ว 7 และปรับการไหลของน้ำตามไฟควบคุม 8
6. เมื่อสร้างโหมดน้ำเดือดคงที่ในภาชนะ Dewar (จะรวบรวมคอนเดนเสท 15-20 ซม. ในกระบอกตวง 9) ให้ดำเนินการควบคุมการรวบรวมคอนเดนเสทตามปริมาณที่ครูกำหนด (V, m 3) . ระยะเวลาของการรวบรวมการควบคุม t, s ถูกกำหนดโดยใช้นาฬิกาจับเวลา
7. ใช้บารอมิเตอร์กำหนดความดันบรรยากาศ Pa, mmHg
8. ป้อนข้อมูลการวัดลงในตารางการสังเกตและเซ็นชื่อโดยอาจารย์
9. เปิดการติดตั้งโดยหมุนสวิตช์ “0” ปิดวาล์ว 7 หมุนที่จับหม้อแปลงอัตโนมัติทวนเข็มนาฬิกาจนกระทั่งหยุด ระบายคอนเดนเสทลงในภาชนะ 3
ตารางที่ 1
|
หมายเลขการวัด |
มม. rt. ศิลปะ. | ||||
การประมวลผลข้อมูลการทดลอง
1. คำนวณปริมาณความร้อนที่ใช้ไปกับการระเหยของน้ำ 1 กิโลกรัม r op, J/kg:
r op = (W - Q) / (Vr),
โดยที่ W = UI - พลังงานความร้อน, W;
Q = 0.04W - การสูญเสียความร้อน, W;
r - ความหนาแน่นคอนเดนเสท kg/m3 เราใช้ r = 1,000 กิโลกรัม/ลูกบาศก์เมตร
2. สมมติว่าน้ำเดือดที่ความดันบรรยากาศ ให้กำหนดค่าตารางของพารามิเตอร์ของน้ำบนเส้นอิ่มตัวและไอน้ำอิ่มตัวแบบแห้งซึ่งป้อนไว้ในตารางที่ 2
ตารางที่ 2
|
ฉัน", กิโลจูล/กก |
S", kJ/(kgK) |
ฉัน", กิโลจูล/กก |
S", เจ/(กก.K) | |||
3. คำนวณค่าพลังงานภายในของน้ำบนเส้นอิ่มตัว u" และไอน้ำอิ่มตัวแห้ง u", kJ/kg โดยใช้สูตร (3) และ (4)
4. คำนวณค่าความผิดพลาด % ของค่าที่พบของความร้อนจำเพาะของการกลายเป็นไอ r op, kJ/kg เทียบกับค่า r ในตาราง, kJ/kg โดยใช้สูตร:
D = (r op - r) 100 / r
5. แสดงกระบวนการที่เกิดขึ้นในภาชนะ Dewar แบบกราฟิกในไดอะแกรม P-v และ T-s
6. สรุปผลการทำงาน
คำถามสำหรับการเตรียมตนเอง
1. การระเหยของของเหลว สาระสำคัญของกระบวนการเดือดและการระเหยของของเหลว
2. กระบวนการไอโซบาริกของการเปลี่ยนของเหลวเป็นไอน้ำร้อนยวดยิ่งในแผนภาพ P-v และ T-s
3. เส้นโค้งขอบเขตที่มีระดับความแห้ง x = 0 และ x = 1 สถานะวิกฤตของสาร
4. แนวคิด: ของเหลวบนเส้นอิ่มตัว ไอน้ำอิ่มตัวแบบเปียก ไอน้ำอิ่มตัวแบบแห้ง ไอน้ำร้อนยวดยิ่ง
5. ความร้อนจำเพาะของการระเหยของของเหลว
6. ระดับความแห้ง ระดับความชื้นของไอน้ำ
7. ตารางคุณสมบัติทางอุณหฟิสิกส์ของน้ำและไอน้ำความหมาย
8. การกำหนดพารามิเตอร์ไอน้ำเปียก
9. แผนภาพ i-s ของไอน้ำ วัตถุประสงค์
10. กระบวนการทางอุณหพลศาสตร์ของไอน้ำในไดอะแกรม P-v, T-s, i-s
รายการบรรณานุกรม
1. วิศวกรรมความร้อน / เอ็ด A.P. Baskakova - ม.: Energoizdat, 1991. - 224 หน้า
2. แนชโชคิน วี.วี. เทคนิคอุณหพลศาสตร์และการถ่ายเทความร้อน- ม.:: บัณฑิตวิทยาลัย, 1980.- 496 น.
3. ยูดาเยฟ บี.เอ็น. อุณหพลศาสตร์ทางเทคนิค การถ่ายเทความร้อน - ม.: อุดมศึกษา, 2541 - 480 น.
4. ริฟคิน เอส.แอล., อเล็กซานดรอฟ เอ.เอ. ตารางคุณสมบัติทางอุณหฟิสิกส์ของน้ำและไอน้ำ - M.: Energia, 1980. - 408 p.
